Ime izdelka:Metil etil keton
Molekularna oblika:C4H8O
Št. CAS:78-93-3
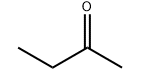
Molekularna struktura izdelka:
Specifikacija:
| Predmet | Enota | Vrednost |
| Čistost | % | 99,8 min |
| Barva | APHA | 8max |
| Kislinska vrednost (kot acetatna kislina) | % | 0,002 maks. |
| vlaga | % | 0,03 maks. |
| Videz | - | Brezbarvna tekočina |
Kemijske lastnosti:
Metil etil keton je zaradi svoje karbonilne skupine in aktivnega vodika, ki meji na karbonilno skupino, dovzeten za različne reakcije. Pri segrevanju s klorovodikovo kislino ali natrijevim hidroksidom pride do kondenzacije, pri čemer nastane 3,4-dimetil-3-heksen-2-on ali 3-metil-3-hepten-5-on. Pri dolgotrajni izpostavljenosti sončni svetlobi nastanejo etan, ocetna kislina in kondenzacijski produkti. Pri oksidaciji z dušikovo kislino nastane diacetil. Pri oksidaciji z močnimi oksidanti, kot je kromova kislina, nastane ocetna kislina. Butanon je relativno stabilen pri segrevanju, toplotna cepitev pri višjih temperaturah pa povzroči enon ali metil enon. Pri kondenzaciji z alifatskimi ali aromatskimi aldehidi nastanejo ketoni z visoko molekulsko maso, ciklične spojine, ketonska kondenzacija in smole. Na primer, kondenzacija s formaldehidom v prisotnosti natrijevega hidroksida najprej proizvede 2-metil-1-butanol-3-on, nato pa dehidrira v metakrilaton.
Do smolničenja pride ob izpostavljenosti sončni svetlobi ali UV-svetlobi. Kondenzacija s fenolom da 2,2-bis(4-hidroksifenil)butan. Reagira z alifatskimi estri v prisotnosti bazičnega katalizatorja, da nastanejo β-diketoni. Acilacija s kislim anhidridom v prisotnosti kislega katalizatorja tvori β-diketone. Reagira z vodikovim cianidom, da se tvori cianohidrin. Reagira z amonijakom, da se tvorijo derivati ketopiperidina. α-vodikov atom butanona se zlahka substituira s halogeni, da se tvorijo različni halogenirani ketoni, kot je 3-kloro-2-butanon, z interakcijo s klorom. Interakcija z 2,4-dinitrofenilhidrazinom povzroči rumen 2,4-dinitrofenilhidrazon.
Uporaba:
Metil etil keton (2-butanon, etil metil keton, metil aceton) je organsko topilo z relativno nizko toksičnostjo, ki se uporablja v številnih aplikacijah. Uporablja se v industrijskih in komercialnih izdelkih kot topilo za lepila, barve in čistila ter kot topilo za odstranjevanje voska. Metil etil keton, ki je naravna sestavina nekaterih živil, se lahko sprošča v okolje zaradi vulkanskih izbruhov in gozdnih požarov. Uporablja se pri izdelavi brezdimnega smodnika in brezbarvnih sintetičnih smol, kot topilo in za površinske premaze. Uporablja se tudi kot aroma v živilih.
MEK se uporablja kot topilo za različne premazne sisteme, na primer vinilne, lepilne, nitrocelulozne in akrilne premaze. Uporablja se v odstranjevalcih barv, lakih, firnajah, barvah v spreju, tesnilnih masah, lepilih, magnetnih trakovih, tiskarskih barvah, smolah, kolofonijah, čistilnih raztopinah in za polimerizacijo. Najdemo ga tudi v drugih potrošniških izdelkih, na primer v gospodinjskih in hobi cementih ter izdelkih za polnjenje lesa. MEK se uporablja pri razvoskanju mazalnih olj, razmaščevanju kovin, pri proizvodnji sintetičnega usnja, prozornega papirja in aluminijaste folije ter kot kemični intermediat in katalizator. Je ekstrakcijsko topilo pri predelavi živil in živilskih sestavin. MEK se lahko uporablja tudi za sterilizacijo kirurške in zobozdravstvene opreme.
Poleg proizvodnje so viri MEK v okolju izpušni plini reaktivnih motorjev in motorjev z notranjim zgorevanjem ter industrijske dejavnosti, kot je uplinjanje premoga. V znatnih količinah ga najdemo v tobačnem dimu. MEK nastaja biološko in je bil identificiran kot produkt mikrobne presnove. Najdemo ga tudi v rastlinah, feromonih žuželk in živalskih tkivih, MEK pa je verjetno manjši produkt normalne presnove sesalcev. V običajnih pogojih je stabilen, vendar lahko pri dolgotrajnem skladiščenju tvori perokside, ki so lahko eksplozivni.
Kategorije izdelkov
-

Telefon
-

E-pošta
-

WhatsApp
-

Zgoraj













